2017年已然过半,我国药品研发“期中”成绩单随之出炉。根据中国新药研发监测数据库CPM的统计,截至6月30日,CDE共承办药品注册申请2117个(按受理号计),如以半年度为统计单位,这一数字相比前一个半年度(2016下半年)增长近40%,仅比上年同期(2016上半年)减少些许(-6%)。药品注册申请量“过山车”似的走势从一个侧面反映了行业对监管政策变化的消化和适应过程。
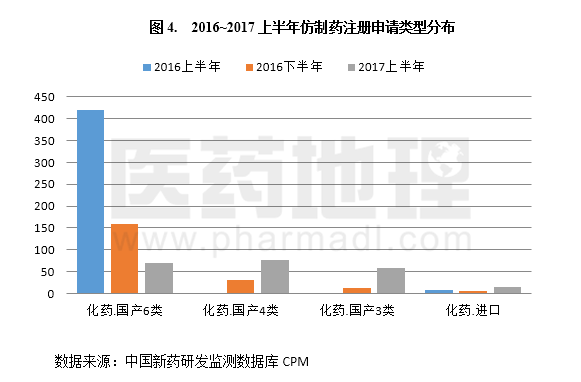
不过,国内药品注册申报形势真如注册申请总量数据那样,仅用半年时间就满血复活?分析一下申请类型构成,就可以发现2017上半年药品注册申请受理量的大幅回升主要得益于补充申请量的增长,2017上半年受理量远超2016年同期水平,估计都是生产工艺核查以及仿制药一致性评价惹的祸。不过,新药申请的贡献仍不容忽视,其2017年上半年受理量虽未恢复至2016年同期水平,但相较于2016下半年增长率达到了近40%(图1)。
IND申报:新报一类化药品种接近2016全年水平
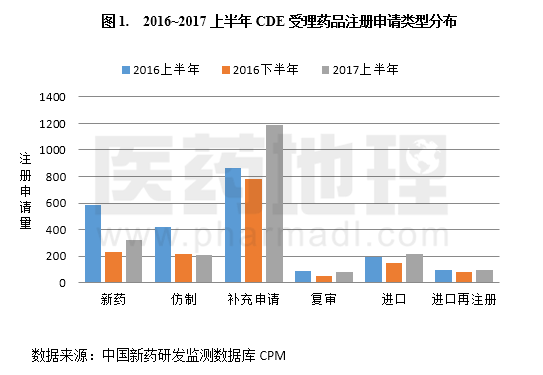
化学药品新注册分类改革实施以后,只有境内外均未上市的药品才可归为新药申报,化学药品新药临床申请和IND申请内涵趋向一致。数据显示,2016年下半年以后,随着时间的推移,新注册分类改革实施受理的注册申请存量逐渐释放完毕,新药临床申请基本上以1类创新药和2类改良药为主了。1类新药定义在注册分类改革前后基本无变化,因此在2016上半年和下半年申报量基本未受影响。然而,进入2017年以来,国产1类化药的申报一拨接着一拨,研发竞赛不断升温(图2)。数据显示,截至6月30日,2017年内首次受理注册申请的新化合物数已达65个,已接近2016年全年的9成。
NDA申报:超越2016同期水平
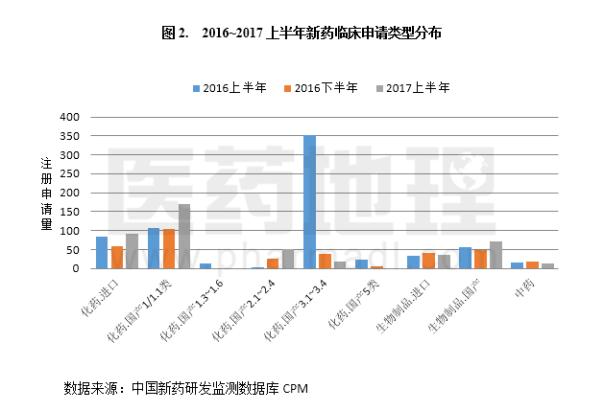
2017上半年,新药上市申请受理合计71件,不仅相比2016下半年翻了一倍,比上年同期(2016上半年)也有增长(10%)。原本受药物临床试验数据核查风暴的影响,自2015年下半年开始,NDA申报量就大幅下滑。再加上2016年3月正式开始实施的化学药品新注册分类改革(3类化药不再按新药管理),2017年上半年能迎来NDA申报量止跌回升实属不易。从申报NDA的品种类型来看,国产1类新药及国产和进口生物制品上市申请量的复苏是关键。

ANDA申报:向左走or向右走?
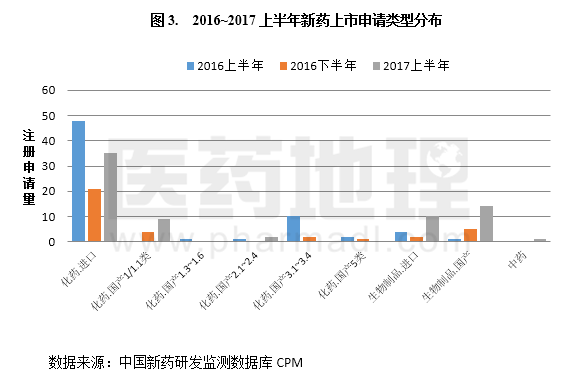
仿制药申报方面,2017上半年受理ANDA申请223件,相比2016下半年微增4%,约相当于上年同期的50%。不过,从新注册分类的受理量来看,增长势头不容小觑(图4),未来仿制药注册申请能否抑制低水平重复冲动,避免注册审批积压问题的再度出现,让我们拭目以待。(作者: 赖树清)