12月4日,君实生物的PD-1单抗JS001(特瑞普利单抗注射液)上市申请率先结束技术审评,进入行政审批阶段。不出意外的话,第一家国产PD-1单抗将花落君实。
众所周知,中国已上市了两款PD-1产品,分别是默沙东的K药和BMS的O药。国产企业中,君实、恒瑞、信达、百济神州4家企业的新药上市申请已被受理且进入优先审评审批程序,此外还有超过50个产品正在进行临床试验,近20个药物申报临床。
这是一个竞争极其激烈的市场。各个玩家进度前后相差仅月余,国内企业与跨国药企上市同类创新药的进度只相差半年,这一方面对于中国创新药是一个里程碑式的事件,代表了中国创新药的能力上了一个新台阶。
另一方面,多个同类产品同时涌入市场,那么先行者抢占市场的优势并不明显,未来的厮杀将依靠企业的综合实力,比如销售能力、临床试验布局、现金流、对终端的把控能力等等。
首家上市的君实生物拥有多少筹码?未来几年PD-1/L1的市场将呈现怎样的厮杀格局?谁将在这个领域占据统治地位?PD-1/L1的价格趋势会怎样演变?
1、国产第一家
实际上,君实生物能成为国产PD-1第一家并不奇怪。特瑞普利单抗是国内第一家向国家药监局提交临床试验申请的PD-1抑制剂产品。
2016年1月1日,特瑞普利单抗获批开展临床试验,2月23日开始首次伦理审查,3月7日,第一个受试者入组。2018年3月,特瑞普利单抗以黑色素瘤适应症上市申请获国家药监局受理,同时在美国开展一期临床试验。
Insight数据库显示,特瑞普利单抗目前有18项临床试验正在开展,其中针对复发或转移性鼻咽癌的三期临床试验为国际多中心试验,此外还有针对黑色素瘤的三期试验在进行,2018年10月18日已经完成第一例受试者入组。四个试验处于二期临床,适应症包括非小细胞肺癌、鼻咽癌、膀胱癌、黑色素瘤;10个临床试验处一期临床阶段。

君实生物的临床试验数据披露也比较全面。从已有数据来看,JS001与百济神州、信达的PD-1单抗都安全性可靠,有效性非劣于O药和K药。
君实生物于2012年12月在上海正式注册成立。其发展模式与一般的生物初创公司“VC+IP+CRO”的发展模式不同,2015年8月13日君实生物在新三板挂牌上市,君实生物先后进行了5次融资,累积13.18亿元。
2018年8月,君实生物向港交所提交上市申请,成为首家“新三板+H股”的公司。
君实生物对自身的定位是通过源头创新来开发首创(First-in-class)或同类最优(Best-in-class)的药物。招股书显示,目前公司的核心管线包括13项在研生物药品。包括七项肿瘤免疫疗法在研药品、两项代谢疾病在研药品、三项针对炎症或自身免疫性疾病药品及一项治疗神经性疾病的药品。其中4项已经获得临床批件,1项已经提交新药上市申请(即特瑞普利单抗)。

君实生物拥有苏州、美国旧金山和马里兰三大研发中心,其中苏州/上海(总部)负责研发、工艺优化、产业化生产和临床试验,旧金山研发中心负责新抗体研发、高通量抗体筛选,马里兰研发中心负责抗体评估、新靶点开发。另外,君实生物在苏州吴江和上海临港设立两个生产基地。
2016和2017年,君实生物的研发投入分别为1.22亿元和2.75亿元,截至2018年4月底,研发投入达到了1.22亿,同比增加96.77%。
从创始团队来看,君实生物总经理李宁曾在美国FDA担任肿瘤产品团队审评员等职务,后在赛诺菲任全球监管事务亚洲监管事务及医学政策副总裁;首席运营官冯辉曾任阿斯利康附属公司MedImmune的科学家,并参与了JS001的专利发明;首席科学官武海曾任安进高级科学家;临床研究运营部副总经理顾娟红曾先后就职于第一三共、默沙东、GSK医疗及药物开发部临床运作主管。
据君实生物招股书显示,截至2018年4月底,公司有347名员工,其中研发和生产的员工占比均为32.3%,18%的员工负责质量控制,负责管理、行政管理、营销的员工人数60人,占比为17%。
可以看到的是,相比于拥有强悍销售能力的恒瑞、由吴晓滨操作商业化的百济神州,目前君实生物并没有来自市场、销售方面的领头人,也没有重金在销售方面进行布局,君实生物的商业化能力目前有待验证。
在合作伙伴上面,君实生物2018年7月11日与石药集团签订《产品合作开发与战略合作协议》。根据协议,JS001将与石药集团的注射用紫杉醇组合开展针对乳腺癌的临床开发。而该协议的签署也许将有助于君实与石药集团开展商业化方面的合作。
2、谁能争霸PD-1市场?
恒瑞、君实、信达、百济神州4家企业的产品都有自身的独特优势,又都有一些小瑕疵,在竞争上互相咬合。
恒瑞的优势在于雄厚的资金实力和产品管线。因此,恒瑞是开展PD-1相关临床试验和探索联合用药最多的企业,恒瑞的另一款PD-L1单抗也已经通过审批审查,凭借在中国肿瘤用药市场的深厚积淀,恒瑞的PD-1产品一旦上市将快速放量。但值得注意的是,恒瑞的SH-1210存在其他PD-1单抗没有的血管瘤副作用,恒瑞在这方面仍需要进一步评估。
信达生物的优势在于产品显著的临床疗效。在针对中国霍奇金淋巴瘤患者的临床试验中,信达的IBI308的疾病控制率相对O药和K药存在明显优势,这是其他PD-1产品不具备的。由此,信达火速通过临床实验阶段,反超君实提交上市申请。但信达曾经撤回上市申请,补充资料重新申报。
百济神州采取肿瘤免疫抑制剂与靶向疗法结合,在协同治疗方面存在更强的组合优势。同时,百济神州与新基在免疫肿瘤领域达成全球战略合作,双方将合作开展多项关键性临床试验,百济神州也是海外进展最快的PD-1单抗药物,但国内的推进进度略落后于其他企业。
在进度最快的适应症方面,已上市的O药获批适应症是二线治疗非小细胞肺癌,K药获批适应症是晚期恶性黑色素瘤。国产4家企业中,恒瑞、信达、百济神州提交的首个适应症都是复发难治性霍奇金淋巴瘤,君实是黑色素瘤,上市初期将与K药共同争夺市场。
3、国产PD-1/L1将打价格战?
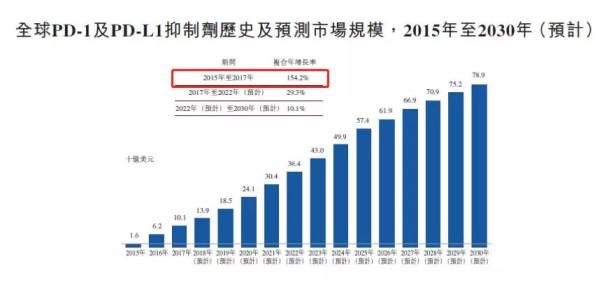
君实生物在招股书中展示了全球和中国PD-1/L1市场规模。全球PD-1及PD-L1抑制剂销售额从2015年的16亿美金上升到了2017年时的101亿美金,复合增速达到了154.2%,预计2017年至2022年复合年增长率为29.3%,市场规模预计在2030年达到789亿美元。但从2017年开始,增长率将会迅速减缓,预计2017年至2022年,复合增长率为29.3%,2022~2030年的复合增长率为10.1%。
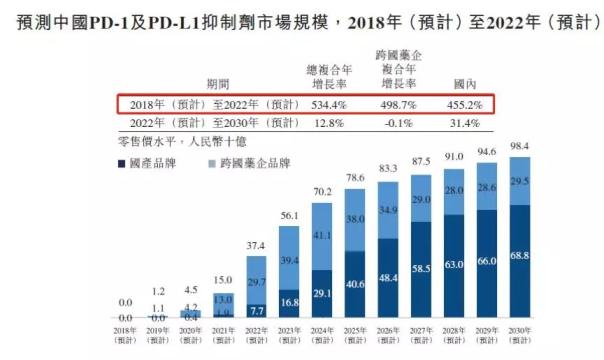
国内PD-1及PD-L1抑制剂市场仍处于发展初期。PD-1/L1抑制剂的市场规模预计将于2018年至2022年期间以534.4%的复合年增长率增长至2022年的374亿人民币。但2022~2030年的复合增长率将缩减至12.8%。
由此来看,该庞大市场能容纳多个重磅产品。但由于后续有几十家PD-1产品都在临床试验阶段,未来PD-1/L1市场唯一的不确定性因素就是价格,如果开展价格战,相关企业前期的巨额研发投入能否收到回报?
近日在一次行业会议上,某本土企业提出这样的问题:K药、O药目前的定价均低于美国、中国香港,这会大大打击国产新药的积极性。
根据公开资料,O药的价格为40mg/10ml 4591元、100mg/10ml 9260元,60kg的患者一个月需要36884元,而在美国则需要66056元。K药的中国零售价为17918元/100mg,全年治疗费用为304606元,仅为美国市场价格的54%。
国产新药会如何定价?
此前,恒瑞医药首席医学官邹建军接受E药经理人采访时曾提到,PD-1单抗作为中国自主研发药物,前期有着高昂的研发投入。在市场投入后,企业会综合考虑中国患者的支付能力,根据企业的市场调研结果,对比同类产品的市场策略,进行科学定价。
而更多的观点认为,几年之后,随着获批产品越来越多,PD-1/L1将不可避免地打价格战。届时,探索更优的组合疗法、布局更前沿的治疗领域是企业的出路。
