作者: 杨昕媛
昨天,一则“武汉大学人民医院(又名湖北省人民医院)关于推进优先使用通过一致性评价药品工作的公告”图片在朋友圈流出。与此前政府层面推进一致性评价相关政策不同的是,这次是药品的直接使用方——医院毫不含糊地指明“对通过一致性评价药品在国家政策框架内予以倾斜”,同时言明“建议临床医师优先开具通过一致性评价药品”。

自2018年4月23日国务院办公厅发布20号文之后,一致性评价节奏在明显加快,各地配套政策也陆续出台,但由于力度不一,给一致性评价的未来添了一些不确定性,而医院层面的真实反应也是关注焦点。此时,湖北省人民医院打响了第一枪。
湖北不是最早一批发布一致性评价后续配套落地政策的省份,但目前来看却是走得最快的省份。医院层面的明确发声使各方看到了政策逐渐渗透到一线的信号。作为医改试点城市之一,武汉湖北省人民医院的这一做法也将被更多的医疗机构效仿。
从更大的层面来看,2018年将是中国药品政策改革与国际接轨的关键一年,仿制药一致性评价是三医联动环节中的重要动作,效仿欧美成熟市场做法、用仿制药替代专利过期原研药的趋势已成定局。近期,《药神》电影引发全国对救命药的讨论,进而上升到加快推进应用我国高质量仿制药的高度,不仅对仿制药在公众层面进行了一次大范围科普,也刺激药企、招标、医保各方行动起来,加速仿制药替代原研的过程,加速当前中国用药结构的调整与蜕变。
三甲医院开始行动了!
截至目前国家药监局已经公布四批共41个产品通过一致性评价。根据目前的BE试验进展、CDE审评审批节奏,2018年下半年将是一致性评价集中爆发的半年。此时,地方配套政策以及医疗机构的真实落地执行情况则成为关注焦点。
截至2018年5月底,有至少11省份出台配套政策,包括招标采购、医保报销、使用等环节。国泰君安给出“力度和进度都好于预期。大部分省份都采取的非常规应对措施,目的是确保通过一致性评价品种,尤其是之前未中标的品种可以进入”的结论。
在促进医疗机构仿制药替代使用层面,国家的整体政策是将通过评价的仿制药纳入与原研药可相互替代药品目录:卫生健康部门要加大对临床用药的监督力度,严格落实按药品通用名开具处方,尤其是在按规定向艾滋病、结核病患者提供药物时,优先使用仿制药。
可以说,国家层面已经给出了大框架。而从地方政策来分析,目前已经有很多信号传递出“力度和进度都优于预期”的趋势。
比如7月16日辽宁省卫计委发布《辽宁加大仿制药采购使用的政策支持力度》,其中提出“对于国家基本药物和肿瘤靶向治疗药物不纳入公立医院药占比计算范畴。”此外,“各级医疗机构在2018年底前,可临时增加采购使用通过仿制药一致性评价的药品。”
药占比是悬在医院头上的一把利剑,对医生用药可谓有着整体调控作用。在此前,部分省份对药占比放开都是针对国家药价谈判品种,辽宁首次在仿制药框架下对基药和肿瘤靶向药提出“不纳入药占比”,将增加医疗机构对通过一致性评价仿制药的使用。
浙江也进行了突破。4月28日浙江省药械采购中心就提出医疗机构在2018年底之前可临时突破《处方管理办法》中“一品两规”的规定,增加采购使用通过一致性评价的产品。
但尽管国家和地方都在号召优先使用,“优先使用”仍然是一个模糊的概念。在4月26日,佛山市《佛山市公立医医疗机构药品采购实施方案(征求意见稿)》曾明确表示不采纳企业提出的“优先采购并在临床中优先选用一致性评价品种”的意见,表示“尊重医疗机构临床选择”,更是给未来趋势增加了不确定性。此外,学术界部分观点认为目前通过一致性评价的仿制药确实与原研药在“临床一致性”方面存在一定差异,如何全方位说服医生、将政策落实到药品使用的真正决策方——医疗机构手里,一直是挑战。
原研药于近期开启的降价潮一定程度上也会给仿制药带来冲击。在国家药价谈判、不纳入医院药占比考核、医保报销、降税又降价等组合拳下,原研药的价格将不再“遥不可及”,再加上市场教育层面还没有对仿制药完全接受,无论是患者还是医生都倾向于选择原研药。仿制药面临的挑战更大。
从这个层面来说,此时三甲医院立场鲜明地表示“在采购政策、临床应用方面给仿制药予以倾斜”,无疑有一个定心丸作用,意味着其在对待原研药和仿制药的态度方面已经出现松动。如果这一做法被更多医疗机构效仿,也就意味着仿制药替代原研药的政策已经渗透到一线,也将鼓励采购、医保等各方相信仿制药能够被医生和患者接受,从而更积极地调动政策制定的积极性。
企业最急迫的任务是什么?
湖北省人民医院的公告还释放出一个信号是:医疗机构给仿制药的定位是“质优价廉”。这也意味着,医院层面或许不能接受通过评价的仿制药涨价的观点。
其实,国家层面对通过评价的仿制药也是持“不能涨价”的态度。国办发[2018]20号文对仿制药提出的是“有升有降、科学合理的采购价格”,对仿制药的表述也是“性价比更高”。从目前各省的落地政策来看,各省都有通过“取多省最低价”的表述,也对价格设定了明确的方向:稳步向下。
企业层面曾多次释放出“通过一致性评价品种应该涨价”的信号。2018年3月12日,浙江华海药业股份有限公司董事长陈保华曾做客新华网、在各个维度提出仿制药在政策上的诉求,其中一条就包括“通过一致性评价产品应该与进口药价格保持一致,或者差不多”。
对于一致性评价品种的定价问题,国泰君安给出的结论是:如果有历史中标记录,考虑到大部分品种相比于原研药价格较低,大张旗鼓涨价难度较大,舆论压力可能也较大。但如果没有历史中标记录,目前价格还没有明确的确定规则。
在价格策略上,国泰君安认为,随着通过同通用名的品种增加,在入围环节壁垒难度较大,也可能面临激烈的竞争,较优的策略是充分考虑竞争对手的情况,选择快速实现挂网,而不是过多纠结于价格。在此之后应抓紧实现入院,快速抢占医院和医生患者资源。而这也正是这一阶段手持一致性评价品种的企业的首要任务。
从日本等成熟市场仿制药替代原研的路径来看,政策攻破医疗机构是促进仿制药替代原研的重要里程碑。2005年规定药房在医生允许变更的情况下可以转换成仿制药、2011年规定私人诊所处方使用通用名给予额外奖励。从市场份额来看,2015年日本整体仿制药替代率由十年前的32%上升到56%。
《我不是药神》电影目前票房已经突破25亿。以这样一种方式,原研药、仿制药的概念在医生和患者层面都做了一次强有力的普及,此前只在医药行业内部流传的一致性评价理念得以被更大范围的人群理解。
在这样的舆论情绪高涨的时刻,对企业来说是绝佳的时机去普及自己的产品、进行市场教育和宣传一致性评价理念,在医生和患者心中建立信任,从而使更多的医疗机构有动力效仿当前湖北省人民医院的做法,为更多政策的落地与执行打下基础。
第五批通过一致性评价品种公布在即
2个月前,国家药监局公布了第四批通过一致性评价的12个品种名单。至此,41个品种已经公布通过一致性评价。
Insight数据库则显示,目前已经有53个品种通过受理号。这也意味着,第五批通过一致性评价的品种将很快公布出来。而根据市场进度,这一批通过品种里不乏重磅抗肿瘤药,部分产品销售额超10亿,企业则包括恒瑞、正大天晴、科伦药业、扬子江、齐鲁制药等大牌企业。
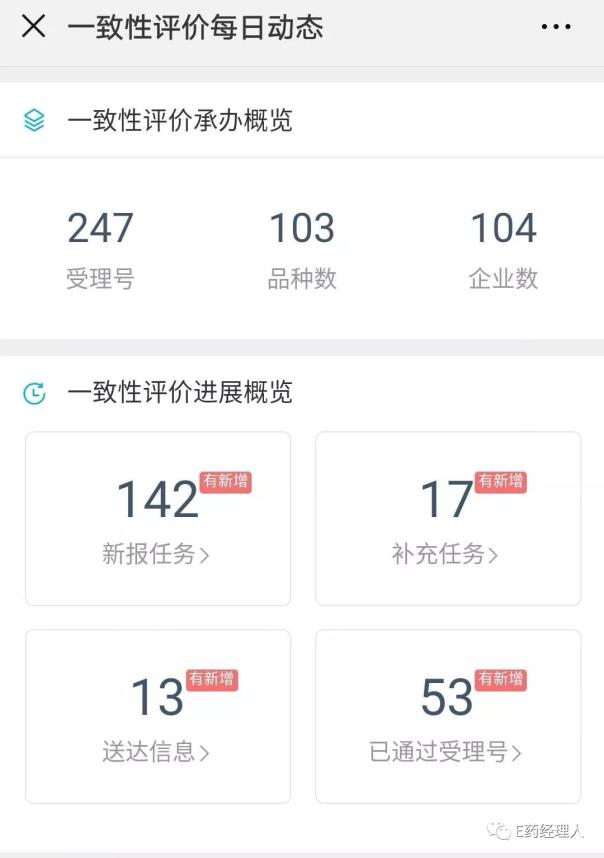
来源:Insight数据库截图
根据公开信息,部分企业其实已经收到国家药监局的一致性评价通过消息。比如,7月16日,江苏豪森伊马替尼仿制药“昕维”通过一致性评价。这正是《药神》电影里的救命药原型,2017年中国公立医疗机构终端和零售药店终端总市场为30.46亿元,豪森药业占比为17.37%,仅次于原研厂家诺华。正大天晴的甲磺酸伊马替尼目前也已经处于审评序列中,米内网预测将在今年年末或明年年初获批。
7月17日一天内,国药集团致君制药的头孢呋辛酯片(0.125g)和新东港药业的阿托伐他汀钙片都通过了一致性评价。前者的0.25g规格的品种已经在第一批通过一致性评价。2017年,这一产品在中国公立医院终端市场销售额17.28亿元,国药致君占比28.67%;后者国内市场接近160亿元,其将与心血管领域重磅品种立普妥和阿乐共同抢占市场。
根据米内网数据,截至7月13日,目前已经通过或视同通过一致性评价、但还未被国家药监局公布的品种中,有4个属于抗肿瘤药,其也最有可能出现在即将公布的第五批一致性评价名单中。

米内网数据库显示,目前已经通过或视同通过一致性评价的仿制药中,有4个属于抗肿瘤药。数据统计截至7月13日。
吉非替尼是另一款口服靶向抗癌药,2017年中国终端市场销售额21.87亿元,92%的市场被原研厂家阿斯利康垄断。齐鲁制药的仿制药伊瑞可已经通过一致性评价,可大大提高这一产品在患者中的可及性。
最不能等的就是患者。患者最期待的消息不是某产品通过一致性评价,也不是相关政策,而是能实实在在吃上高质量、高性价比的产品。这也催促着手持一致性评价通过品种的企业尽快有所动作,加速产品的临床使用。同时,在一致性评价中走得最快的这一批品种的市场表现也会被后来者紧紧盯着,从而影响后者的积极性。从这个意义上说,先行者更有责任和使命理顺各方关系,利用现有政策建立好市场规则,加速迎接即将到来的仿制药替代时代。
