2016年,美国FDA批准了22款新药,数量为近10年来的最低。今年年初,许多业内资深人士估计,今年的获批新药数会出现强势反弹,事实也证明了他们的判断。2017年至今不满6个月,美国FDA已经批准了23款新药,超过了2016年的总和。在这6月的尾声,我们也结合美国FDA的数据,为各位读者送上今年上半年获批新药的信息。

获批新药数创多项纪录
生物技术与医药行业在过去的6个月中充满活力。据统计,自2011年以来,还从未有哪一年的上半年,能够有超过20款新药得到批准。今年上半年的数据打破了这一纪录。出色的成绩背后,有着多个潜在的推动因素。首先,随着业界对科研和新药研发的持续大量投入,创新疗法层出不穷,人们也得以在小分子新药的领域外,开拓新的疆界。以生物药为例,在2016年之前,每年上半年由美国FDA批准的单克隆抗体新药不超过3款。而今年上半年的获批单克隆抗体新药数为6款。这是飞速成长的生物药领域的一个缩影。值得一提的是,这同样是自2011年以来的一个纪录。
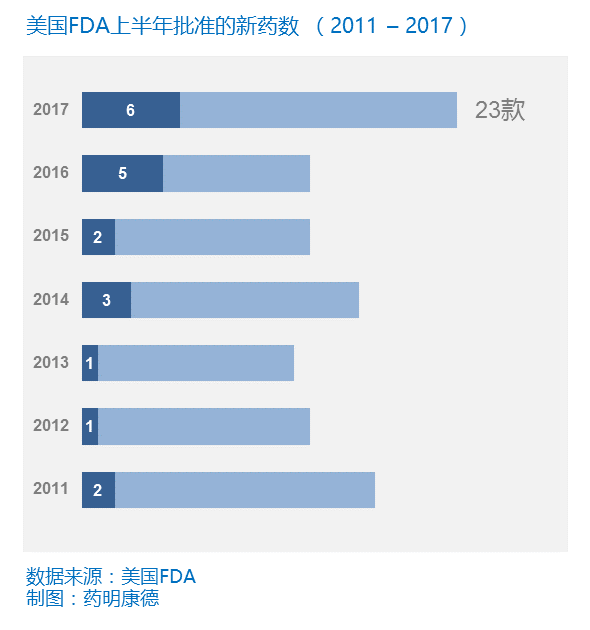
▲今年上半年,美国FDA批准了23款新药。这是近年来的一个纪录。其中,今年上半年获批的单克隆抗体数(深蓝色)为6款,同样是近年来的最高
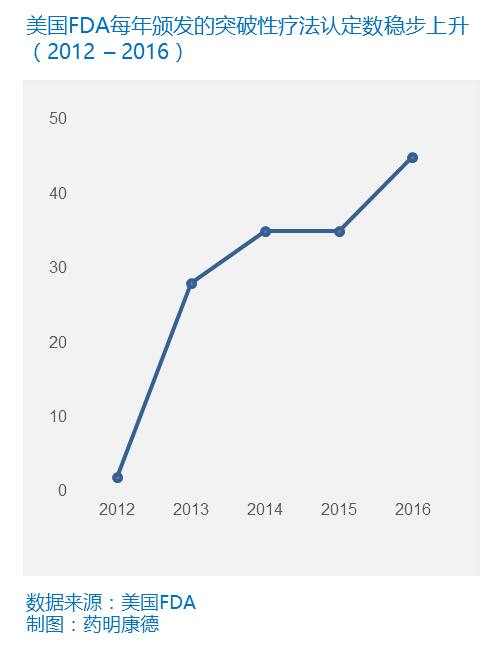
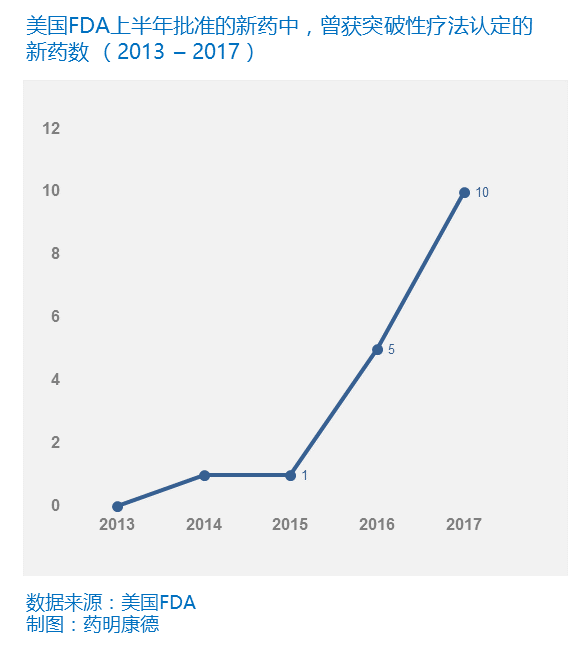
其次,今年上半年的获批新药数出现明显增长,也与“突破性疗法认定”等加速政策有关。2012年7月,美国FDA推出了“突破性疗法认定”,宣布只要一款新药能够治疗严重危及生命的疾病,并且先期的临床数据表明该药在一项或多项重要的临床终点上较现有疗法有显的改善,即可获得这一荣誉,并随即在审评的流程中享受“加速”。在2012年至2016年期间,每年美国FDA颁发的突破性疗法数不断增长,这也让越来越多的突破性新药得以提前问世。今年上半年,前人的努力终于迎来了收获。在获批的23款新药中,有高达10款新药曾获得突破性疗法认定。未来,我们也将继续享受这一政策带来的利好。
抗癌明星疗法持续火热
抗癌新药一直是新药研发的重头,并占去了每年的获批新药中,相当大的一部分比例。今年上半年,美国FDA一共批准了6款与癌症治疗相关的新药,数字是2011年来的最高。这与近年来层出不穷的抗癌新疗法有关。
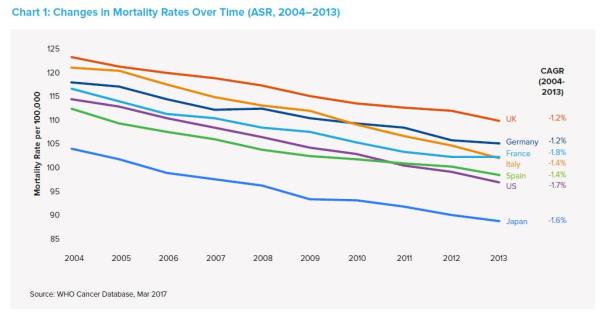
▲随着抗癌新疗法的问世,全球的癌症患者死亡率持续下降(图片来源:QuintilesIMS Institute)
在PD-1/PD-L1通路的抑制剂上,今年上半年我们看到了两款新药的问世。由德国默克(Merck KGaA)与辉瑞(Pfizer)带来的Bavencio(avelumab)与由阿斯利康(AstraZeneca)带来的Imfinzi(durvalumab)均是抗PD-L1的单克隆抗体,分别用于转移性梅克尔细胞癌(metastatic Merkel cell carcinoma)和晚期或转移性尿路上皮癌的治疗。基于肿瘤免疫疗法的出色疗效,这两款新药均得到了美国FDA颁发的突破性疗法认定,以及优先审评资格。最终,这两款新药也都获得了加速批准(Accelerated Approval),体现了这一领域的持续火热。
另一些获批的抗癌新药针对的同样是近年来的热门靶点。药明康德合作伙伴Tesaro的Zejula(niraparib)是一款PARP抑制剂,在多个癌症患者群体中均能起到良好的疾病控制效果;由诺华(Novartis)带来的乳腺癌新药Kisqali(ribociclib)是广受关注的CDK4/6抑制剂;武田(Takeda)集团子公司ARIAD Pharmaceuticals研发的新药能治疗ALK阳性的非小细胞肺癌患者;诺华的另一款新药Rydapt(midostaurin)则能治疗急性骨髓性白血病,是近25年来取得的重大突破。不少分析人士认为,这些获批新药中的大多数,会在未来成为重磅新药。
