爱尔兰制药巨头Allergan(艾尔建)6月11日公布了一项用于评估其口服药物Atogepant有效性、安全性以及耐受性的2b/3期临床试验CGP-MD-01的积极结果。在12周的时间里,间歇性偏头痛患者的平均月偏头痛/疑似偏头痛(MPM)头痛天数与安慰剂相比具有统计学意义上的显著减少,所有剂量和剂量方案的积极治疗组的数据都达到了主要终点。
Atogepant是继ubrogepant之后艾尔建第二个在研口服降钙素相关基因肽(CGRP)受体拮抗剂,主要用于预防偏头痛。CGRP及其受体参与偏头痛病理生理学有关的神经系统区域中表达。Atogepant与用于偏头痛急性治疗的口服CGRP受体拮抗剂ubrogepant具有化学差异,前者具有更高的效力和更长的半衰期,使其非常适于偏头痛的预防性治疗。今年年初艾尔建公布了两项关于ubrogepant的关键性3期临床试验的积极结果。目前,公司会和监管部门讨论后继续推进Atogepant的试验。
CGP-MD-01是一项在美国开展的2b/3期的多中心、随机、双盲、安慰剂对照的平行对照试验。该研究包括在随机化之前4周筛选/基线周期,随后的12周的双盲治疗期;以及另外4周的安全性随访期。入组标准包括:病人年龄为18-75岁,包含具有先兆性或非先兆性偏头痛至少1年的病史;并且在最近3个月内和28天的基线周期内平均月偏头痛/疑似偏头痛(MPM)头痛天数在4-14天之间。主要有效性终点是在12周的治疗周期里平均月偏头痛/疑似偏头痛(MPM)头痛天数基线的变化。
数据显示,与基线相比,所有积极治疗组的主要疗效参数均显示统计学显着降低(见表一)。试验其他终点的更加详尽的内容预计将会在随后的科学会议进行介绍。
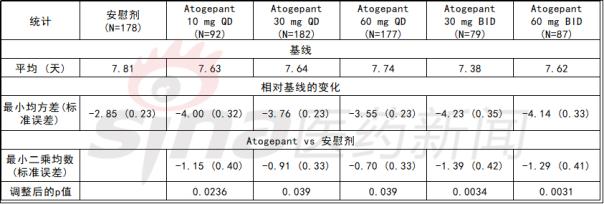
CGP-MD-01中,Atogepant呈现出良好的耐受性。试验中最常见的不良反应是恶心,乏力,便秘,鼻咽炎和尿路感染,这些事件在至少1个治疗组中的频率>5%,并且高于安慰剂组。在这一每天一次总共12周的试验中,并没有出现肝脏毒性信号。该药物的肝脏安全数据与安慰剂对应的数据非常接近。
艾尔建首席研发官David Nicholson说,“非常高兴和大家分享研究的积极结果,Atogepant是我们第一个处于2b/3临床阶段的间歇性偏头痛研究药物,它昭示着口服剂型——这一在偏头痛预防领域还未实现的治疗方法的巨大机遇。”
艾尔建首席商务官Bill Meury说,“这些积极的研究结果说明与其他已上市或正在开发中的的治疗方案相比较,口服Atogepant预防偏头痛的效果更具吸引力,我们也对该产品的商业化前景充满期待,并且正往到下一阶段快速推进。随着Botox获批用于慢性偏头痛,以及口服Atogepant和ubrogepant用于偏头痛的预防和快速治疗,艾尔建拥有目前业界最具创新性和深度的偏头痛产品线。”
“这些积极数据体现了Atogepant作为偏头痛患者广谱用药的潜能。跨越剂量和剂量方案的有效性和安全性也使得Atogepant在大量未满足治疗需求的患者群体中显示出良好的前景。”伦敦国王学院、加州大学旧金山分校神经学家和教授Peter Goadsby博士说道。“该试验结果不但为口服CGRP拮抗剂的临床潜力提供了持续凭证,而且对继续开展研究和开发针对偏头疼患者新疗法具有重要的实质价值。”
偏头痛(migraine)是临床最常见的原发性头痛类型,是一种常见的慢性神经血管性疾患,多起病于儿童和青春期,中青年期达发病高峰,女性多见。临床以发作性中重度、搏动样头痛为主要表现,头痛多为偏侧,一般持续4-72小时,可伴有恶心、呕吐,光、声刺激或日常活动均可加重头痛,安静环境、休息可缓解头痛。(新浪医药编译/Jason)
文章参考来源:Allergan's Oral CGRP Receptor Antagonist Atogepant Demonstrates Robust Efficacy and Safety in Episodic Migraine Prevention in a Phase 2b/3 Clinical Trial
