作者:Tumour
2018年8月20日,拥有ImmTAC平台技术的Immunocore公司宣布,其与葛兰素史克(GSK)合作的首个ImmTAC分子IMCnyeso已对首个病人进行给药实验,表示其临床I期实验已正式开始,该研究将评估IMCnyeso在NY-ESO-1 和/或LAGE-1A阳性的非小细胞肺癌(NSCLC)、膀胱癌、黑素瘤和滑膜肉瘤患者中的安全性和耐受性。IMCnyeso是Immunocore公司第二个进入临床实验的ImmTAC分子,其首个ImmTAC(IMCgp100)目前已获得FDA孤儿药认证用于治疗葡萄膜黑色素瘤。
医药界大咖云集ImmTAC
Immunocore公司成立于2008年, 拥有全球独有的ImmTAC技术,其作用机理类似于靶向CD3的双特异性抗体,能招募T细胞来攻击具有特定抗原呈递的肿瘤细胞,被众多大型制药公司所看好,目前,Immunocore已与阿斯利康、基因泰克、葛兰素史克以及礼来等公司达成了广泛的合作,利用 ImmTAC开发针对癌症的新型治疗方法。近期,比尔和梅林达盖茨基金会投资了4000万美元,用于支持针对传染病的ImmTAV和ImmTAB 疗法的发展。

图1:与Immunocore合作的公司和机构
什么是ImmTAC技术平台?
ImmTAC是一种新型的双特异性生物分子,它由抗CD3(scFv)和一种亲和增强的T细胞受体(TCR)两部分组成(图2),在靶向特定肿瘤表面呈递抗原肽的同时激活有效和特定的T细胞反应来识别和摧毁肿瘤细胞。
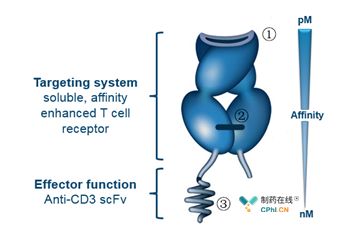
图2:ImmTAC分子形式
ImmTAC的设计来源于天然的人类TCR,涉及三个专有的工程化核心技术(图2):
① TCR高亲和力增强。在自然界中,识别癌症抗原的TCRs通常对其相应的抗原有微弱的亲和力,这意味着癌症细胞本质上是免疫系统不可见的。癌症细胞对pHLA的下调进一步加剧了这一问题。为了解决这一问题,ImmTAC的TCR使用噬菌体展示进行了150万倍的亲和力增强,得到了pM级的亲和力TCRs。这种高亲和力的识别意味着,免疫系统分子可以有效地识别出癌症细胞。
② 构建可溶和稳定的TCRs。使用TCRs作为治疗的一个主要障碍是在作为可溶性蛋白质TCR极不稳定。通过使用一种新型的二硫键,使TCRs在溶液中保持了稳定的状态。新的二硫键被埋在TCR的核心,降低了免疫原性的风险,并通过结晶学研究显示这种结构不改变自然的TCR结构。
③ T细胞重定向效应功能。癌症细胞所呈现的pHLA复合物的数量很少,这意味着T细胞重定向效应功能需要特别有效。通过将改造的TCR与抗CD3抗体片段(scFv)融合在一起,免疫系统分子能够接触到天然T细胞激活途径,在癌细胞表面只有5-10个pHLAs的情况下,也可实现对癌细胞的有效T细胞重定向。
ImmTAC不仅可以在高产低成本的细菌表达系统中制造,而且稳定性高,保质期可达数年之久。另外,它的候选靶点也是相当广泛。
ImmTAC杀伤肿瘤机理

图3:ImmTAC的作用机理
图3显示了一个ImmTAC的作用机理和过程。ImmTAC识别并结合到肿瘤细胞表面peptide-HLA(1)。ImmTAC的自由端(一个anti-CD3抗体片段)招募或重定向循环T细胞至肿瘤(2)。这样,ImmTAC就架起了癌症细胞和T细胞之间的一座桥梁,形成免疫突触(3), 激活T细胞并释放溶解性颗粒,导致癌症细胞的死亡(4)。
ImmTAC优势
ImmTAC不仅可以在高产低成本的细菌表达系统中制造,而且稳定性高,保质期可达数年之久。
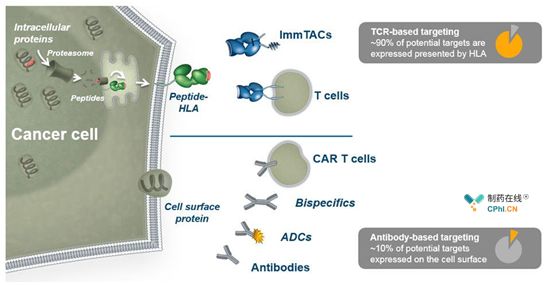
图5:相对于抗体ImmTAC候选靶点更加广泛
另外,它的候选靶点也是相当广泛。细胞表面90%的抗原,位于MHC-I抗原肽复合物中,仅有10%可以作为抗体类药物的潜在靶点。而基于T细胞受体的ImmTAC,其潜在靶点大约为抗体类药物的9倍,筛选出针对肿瘤特异性抗原药物的概率大大增加,有效性和安全性的问题也有了最大限度的保障。
图文来源:http://www.immunocore.com/
原标题:GSK首个ImmTAC开始病人体内实体瘤临床I期实验 大咖云集的ImmTAC你真了解吗?
